교육 2022 서울바이오허브 제1차 의약품 RA(인허가) 전문가 양성 과정 교육생 모집

-
행사기간
2022-05-18 ~ 2022-06-15
-
신청기간
2022-05-04 ~ 2022-05-13
-
장소/시간
서울바이오허브 산업지원동 컨퍼런스홀A / 13:30~17:30
-
모집대상
서울바이오허브 입주기업 재직자 및 서울시 소재 바이오 분야 (예비)창업기업 관계자, 취업준비생 등
-
모집인원
35
서울바이오허브에서 서울시 소재의 바이오 분야 (예비)창업기업의 전문인력 양성을 위해
'2022 서울바이오허브 제1차 의약품 RA(인허가) 전문가 양성 과정' 을 개최합니다.
많은 관심과 참여 부탁드립니다.
[※본 교육은 별도의 수료증 발급이 없는 교육입니다.]
□ 개요
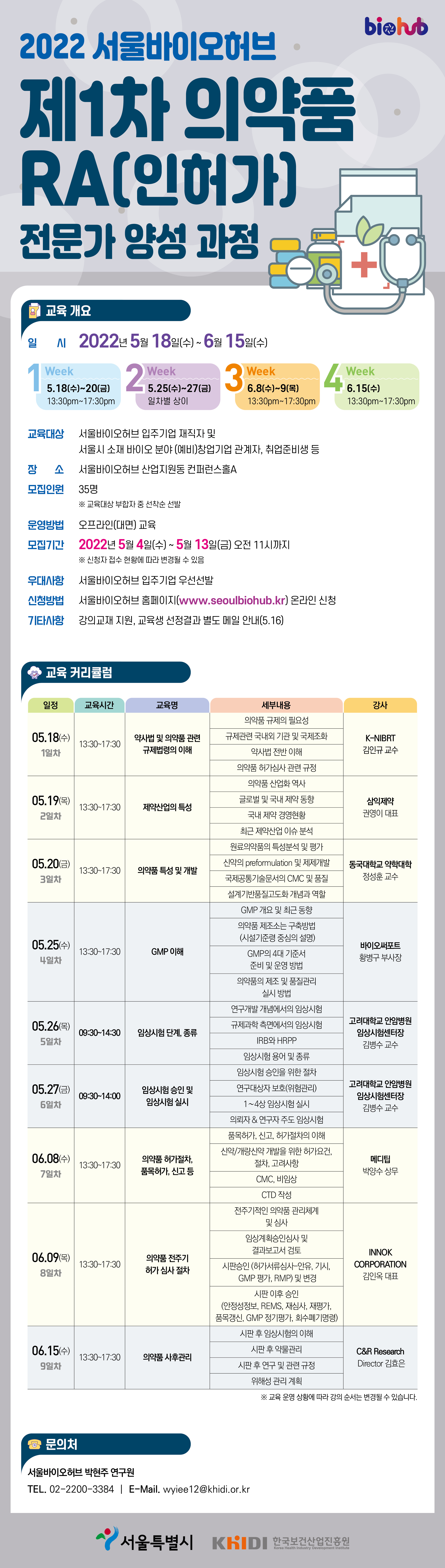
○ 교육과정명 : 2022 서울바이오허브 제1차 의약품 RA(인허가) 전문가 양성 과정
○ 교육대상 : 서울바이오허브 입주기업 재직자 및 서울시 소재 바이오 분야 (예비)창업기업 관계자, 취업준비생 등
○ 일 시 : 2022년 5월 18일(수) ~ 6월 15일(수)
1주차 | 5.18(수)∼20(금), 13:30~17:30 | |
2주차 | 5.25(수)∼27(금), 일차별 상이 | |
3주차 | 6.8(수)∼9(목), 13:30~17:30 | |
4주차 | 6.15(수) 13:30~17:30 |
○ 장 소 : 서울바이오허브 산업지원동 컨퍼런스홀A
○ 모집인원 : 35명
※ 교육대상 적합자 중 선착순 선발
○ 운영방법 : 오프라인(대면) 교육
○ 모집기간 : 2022년 5월 4일(수) ~ 5월 13일(금) 오전 11시까지
※ 신청자 접수 현황에 따라 변경될 수 있음
○ 우대사항 : 서울바이오허브 입주기업 우선선발
○ 신청방법 :
- 서울바이오허브 홈페이지(www.seoulbiohub.kr) 온라인 신청서 제출
○ 기타사항 :
- 강의교재 지원
- 교육생 선정결과 별도 메일 안내(5.16)
○ 주의사항 : 노쇼방지 등을 위해 교육생 선정 후 무단불참 및 당일취소 시 추후 서울바이오허브에서 운영하는 모든 교육에 참가가 제한될 수 있습니다.